
人工智能助力药物发现:大型制药公司争相竞逐的新赛道

包括瑞士罗氏(Roche)和诺华(Novartis)在内的制药巨头,正将大笔资金投入人工智能以研发新药,用于治疗各类疾病。然而,要让人工智能发现的药物造福患者,依然任重道远。
閱讀本文繁體字版本請 點擊此處
点击这里,订阅瑞士资讯swissinfo.ch时事通讯(Newsletter),迅速、深入、互动地了解瑞士第一手新闻资讯。
马蒂亚斯·施泰格(Matthias Steger)发现了治疗视网膜色素变性(一种罕见的退行性眼病)的候选药物EA-2353,但整个发现过程“科技含量很低”:只用了一个笔记本和一支铅笔。
作为训练有素的药物化学家,施泰格近十年来一直记录那些对干细胞-前体细胞(可在受损组织中再生的细胞)有影响的化学结构。要从这些化学结构中找到潜在的候选药物,他需要找出其中的规律,这一过程要花费多年时间和大量资金在实验室进行测试,结果往往充满不确定性。在自主创业之前,施泰格曾在罗氏公司从事了10年药物研发等工作。
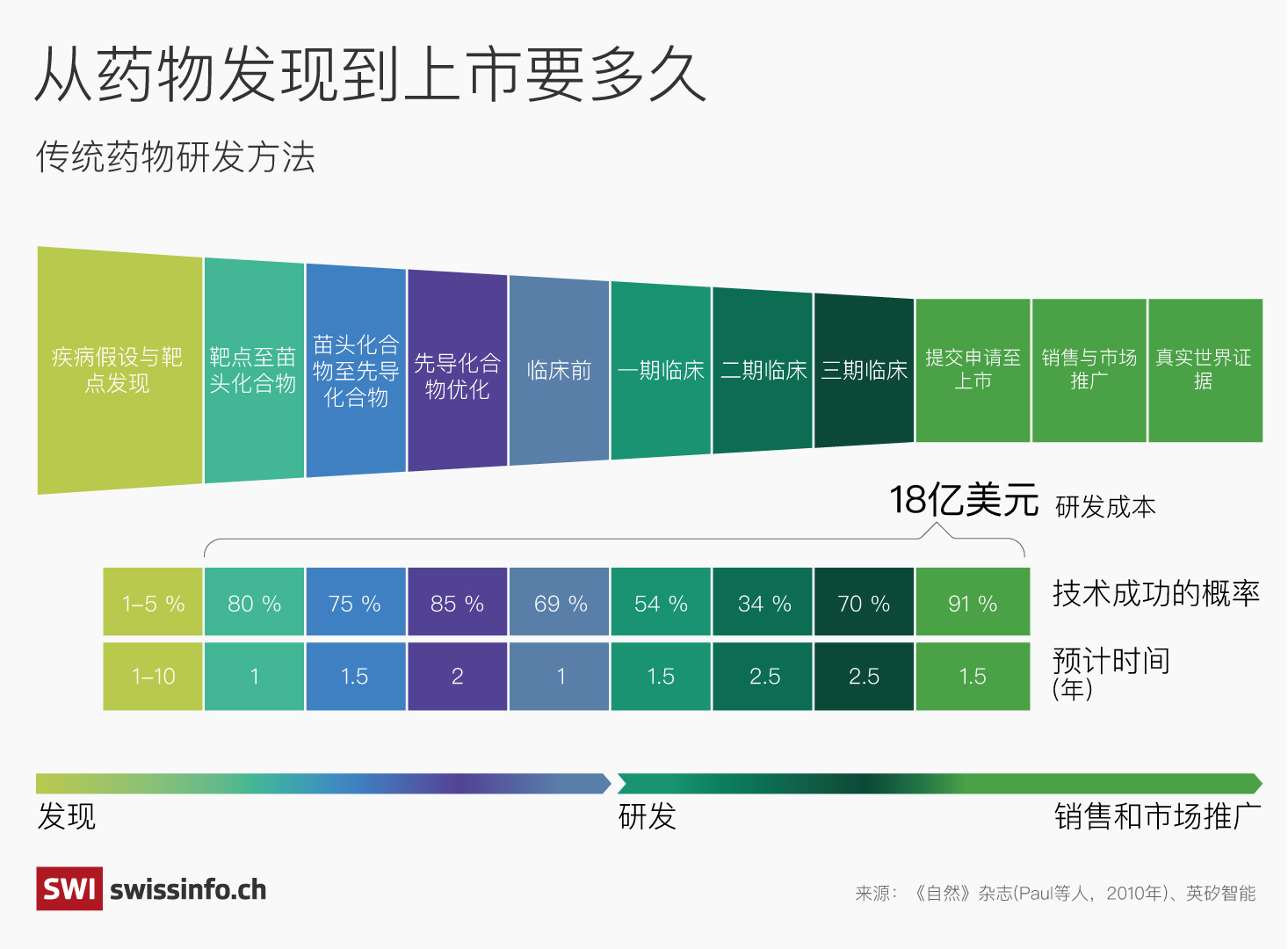
施泰格对瑞士资讯swissinfo.ch表示:“发现一个新分子,犹如大海捞针。即便对于一名训练有素的化学家,也免不了要凭借直觉去尝试。”通常来说,一个新药从研发到上市,平均需要十年时间和约25亿美元(约合人民币181亿)的投入。
为了加速这一过程,他将化学结构发送给了吉斯伯特·施耐德(Gisbert Schneider),施耐德是他在罗氏公司的前同事,目前在瑞士苏黎世联邦理工学院(ETH Zurich)教授计算机辅助药物设计。施耐德利用自己开发的人工智能模型,根据这些化学结构中的规律,识别出具有所需生物活性的分子。施泰格和他的团队对这些分子进行了几年的测试和合成,最终研发出两种候选药物,其中一种是EA-2353,现已进入早期临床试验阶段。
施泰格表示:“如果没有人工智能,我们或许难以找到这个候选药物。”他和施耐德于2016年成立了初创公司Endogena,该公司在苏黎世和旧金山设有办事处,致力于进一步开发这两种候选药物。“算法能洞察人眼发现不了的规律。”
人工智能在候选新药的发现中展现出巨大潜力,其时间和成本仅为传统方法的一小部分,这推动了人工智能投资热潮。波士顿咨询公司去年发布的一份研究报告显示,过去十年间,投资者已向大约200家“AI优先”生物技术公司和初创企业投入了180多亿美元,这些公司和初创企业将人工智能作为药物发现工作流程的核心。
这些初创企业和科技公司一直走在技术的最前沿,但随着人工智能发现的药物进入人体试验阶段,包括瑞士巨头罗氏和诺华在内的更多大型药企正在争先恐后地抢占先机。
去年,罗氏宣布与美国芯片制造商英伟达(Nvidia)开展多年期研究合作,以加快药物发现,这是罗氏自2019年以来签署的至少八项人工智能合作协议之一。今年1月,瑞士制药公司诺华向谷歌DeepMind的子公司Isomorphic Labs支付了3’750万美元的预付款,如果它在开发三种候选新药方面达到某些里程碑,还将获得12亿美元的付款。在过去十年中,制药公司与人工智能药物发现初创公司之间达成了100多项交易,这些只是其中的一小部分。
搭上发展快车
几十年来,大型制药实验室一直在使用计算机辅助药物开发,但直到现在,还有人对过于依赖人工智能持保留态度。
施耐德说:“多年前我们尝试过使用人工神经网络,但在21世纪前十年,制药公司普遍觉得人工智能并未带来预期的效果。这些早期网络或人工智能缺乏必要的精细度,同时也缺少足够的数据和强大的计算机来执行海量计算。
如今,这种观念已经发生了转变。“现在,人们更愿意接受人工智能算法提出的建议,没有一家制药公司甘于落在后面。”
人工智能指的是一系列高级计算和建模技术,这些技术通常从大量复杂的数据源中进行分析和学习,并能以超出人类能力的数据处理规模和速度产生分析结果,或执行通常需要人类智能水平才能完成的任务。深度学习利用人工神经网络从数据中提取知识,是药物发现中常用的人工智能技术。
资料来源:波士顿咨询公司
这一转变的背后是近年来深度学习、生成式人工智能工具(如ChatGPT)、算力以及遗传学和分子生物学知识的快速发展。
最新一代的人工智能模型可以从大量不同的数据集甚至图像中分析和发现规律,这对药物发现极为有用,因为科学家们需要面对数万亿个细胞和每个人体内约2万个基因。
2020年,谷歌的人工智能研究子公司DeepMind推出了AlphaFold,这是一种可以预测人类蛋白质、RNA和DNA三维结构的人工智能算法。AlphaFold在确定SARS-CoV-2的蛋白质结构方面发挥了重要作用,帮助科学家以创纪录的速度研发出新冠疫苗。
AlphaFold不仅推动了大量新药靶点的研究,而且证实了人工智能在造就科学突破方面的潜力。目前,市面上有许多专有和开源的人工智能软件工具,被制药公司用来搜索医学期刊的相关数据、筛选分子库中有潜力的候选药物,以及确定疾病靶点。一些研究表明,人工智能可以将药物发现的时间和成本减少25%到50%。
“人工智能,包括机器学习和大型语言模型,并不是全新的技术,”位于巴塞尔的罗氏公司研发部门计算科学产品负责人埃利夫·奥兹基里姆利(Elif Ozkirimli)说,“但在过去两年中,其应用和规模增长都大大加速。”
根据最近的一份投资者交流活动演示文稿,罗氏每年投入约30亿美元,用于彻底改造公司的数字基础设施,并使人工智能深度融入其研发流程。几年前,罗氏从麻省理工学院和剑桥大学聘请了顶尖的计算生物学家,在其位于旧金山的子公司基因泰克(Genentech)的计算科学部门组建了一支约400人的团队。此外,还有数百名这类专业人员在巴塞尔和其他地点工作。
2021年,罗氏收购了纽约一家三人初创企业Prescient Design,创建了一套算法。这套算法利用公开数据以及罗氏从实验和临床试验中获得的专有数据进行训练。这套算法已被用于为老药寻找新的适应症,并优选管线中成功几率最高的候选药物。
从搜寻到创造
除了提高药物发现的效率,人工智能还有可能识别甚至创造化学家未曾想象过的分子。有些算法,如施耐德用于Endogena的算法,甚至可以从零开始创造出新的分子。
施耐德向瑞士资讯表示:“我们不再需要一个接一个地筛选分子来寻找药物,生成式人工智能正在彻底改变药物发现的过程。它使我们能够设计出具有特定属性的分子,而不是四处寻找。”
一些初创公司已经开始了相关探索。总部位于香港的初创公司英矽智能(Insilico)利用人工智能模型识别出肺纤维化(一种严重的肺病)的药物靶点,并创造了类似药物的分子结构。该候选药物的发现历时18个月,耗资300万美元,远低于传统方法,目前正处于二期临床试验阶段。2022年,英矽智能与法国制药巨头赛诺菲签署了一项价值高达12亿美元的协议,旨在识别疾病靶点并推进候选药物的发现。
基因泰克公司的化学家和计算科学家开发了一种名为GNEProp的深度学习框架,用于识别针对“超级细菌”(对抗生素产生耐药性的细菌)的小分子抗生素。有些由该算法产生的分子,其结构与训练模型时使用的分子截然不同。
这家公司正在将一些分子推进到临床前阶段,同时利用实验室研究结果重新训练人工智能模型,以便模型在未来做出更准确的预测。
奥兹基里姆利说:“药物发现需要不断试错。有了人工智能,我们尝试将部分试错过程纳入机器学习模型,使其能够做出更好的预测。”
马拉松而非短跑冲刺
尽管投资巨大,对新药发现的热情高涨,但制药公司在宣扬人工智能的成就方面仍持谨慎态度。罗氏和诺华并未公开任何正处在临床试验阶段由人工智能发现的药物名称。计算机屏幕上的成功,甚至实验室里的成功,并不总能预示药物最终会在患者身上取得成功。
药物研发的失败率极高:传统方法发现的药物中有90%会在临床试验阶段失败。在这一阶段,药物的安全性和有效性将在人体中进行测试。现在断言人工智能发现的药物是否会有更好的表现还为时尚早,同样,哪些人工智能算法能做出最准确的预测也尚未可知。

相关内容
大型制药公司扎堆的瑞士正努力吸引人工智能初创企业
苏黎世联邦理工学院的施耐德向瑞士资讯指出:“关于人体生物学、疾病的演变以及为什么有些患者对药物的反应比其他人更好,我们还有很多不了解的地方。现在有一种过度夸大人工智能工具潜在益处的倾向,因为我们在研究人体生物学时忽视了其中不可预测的混沌因素。”
根据今年4月发表的一项研究,过去十年里,由使用人工智能进行药物发现的公司开发的药物中,至少有75种候选药物进入了临床试验阶段。在通过一期临床试验的候选药物中,约有80%-90%获得了成功。这一比例高于50%-60%的行业平均水平。
然而,一些专家对研究方法提出了质疑,认为人工智能在这些药物设计中的应用程度差别很大,因此很难一刀切地说人工智能是否成功。此外,二期临床试验往往是药物能否上市的更大决定因素,在这个阶段会有更大的患者群体进行用药试验。
一些候选药物已经遭遇挫折。去年10月,一家名为Exscientia的初创公司宣布,它将终止其基于人工智能的癌症候选药物EXS-21546的早期临床试验。几个月前,总部位于伦敦的BenevolentAI公司的另一种人工智能设计药物在早期试验中的疗效低于预期。
“大多数药物的失败并不是因为分子出了问题。很多时候,分子确实按预期起效,”西格说,“真正的问题在于,分子生物学机理与患者自身病理之间的联系,并没有按照假设那样发展。”
(编辑:Virginie Mangin/ds,编译自英语:瑞士资讯中文部/gj)

符合JTI标准





























您可以在这里找到读者与我们记者团队正在讨论交流的话题。
请加入我们!如果您想就本文涉及的话题展开新的讨论,或者想向我们反映您发现的事实错误,请发邮件给我们:chinese@swissinfo.ch。