La pharma moins mobilisée sur la Covid-19 que le secteur public
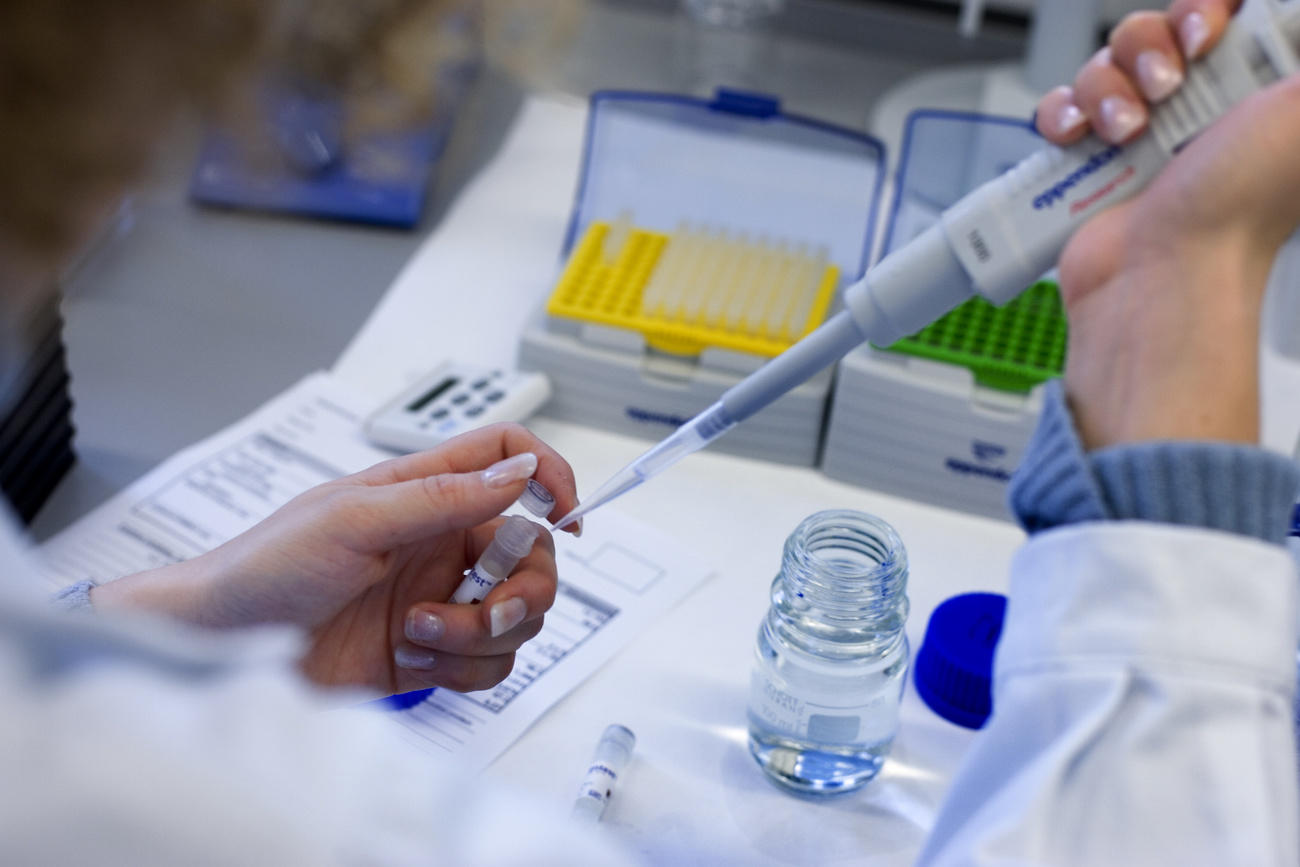
L'industrie pharmaceutique est souvent présentée comme le fer de lance pour trouver un remède à la pandémie. Pourtant, côté traitement, le poids de la recherche est largement supporté par d'autres institutions, majoritairement publiques.
Gilead et son Remdesivir, Sanofi ou Novartis et la controversée Hydroxychloroquine, Roche et son Actemra: depuis le début de la crise du coronavirus, ces grands noms de la pharma sont apparus comme source possible de traitement, avant que la plupart des espoirs qu’ils portaient ne soient douchés.
Aujourd’hui, un traitement totalement efficace reste à trouver. Si l’industrie semble avoir focalisé les espoirs, une analyse de la RTS sur les études ciblant le virus montre que ce n’est pas du côté de la pharma que les plus gros efforts sont menés pour trouver un médicament.
Effort limité de l’industrie
Depuis le début de la crise, 421 essais cliniques de phases 2 et 3 sur des médicaments ont été recensés par l’OMS et les autorités américaines (hors-vaccin et appareils techniques). Ces phases correspondent aux dernières étapes de test sur les humains, avant utilisation à grande échelle.
Seul un essai sur cinq est conduit par un entreprise pharmaceutique, de manière indépendante ou en collaboration avec d’autres acteurs. Par rapport à l’ensemble des essais de phase 2 et 3 menés en 2019, la part de l’industrie dans ces études est réduite de moitié.
Cette faible présence des pharmas ne surprend pas Ellen ‘t Hoen, directrice de Medicines Law and PolicyLien externe. « L’attitude de l’industrie était tout à fait frappante en début d’épidémie. Pour s’impliquer, leur message était ‘nous voulons plus d’argent' », explique cette spécialiste des questions de santé et de propriété intellectuelle.
Invitée à réagir à ces chiffres, Interpharma, l’association des entreprises pharmaceutiques suisses, ne souhaite pas les commenter mais affirme qu’il existe actuellement « une collaboration sans précédent entre les entreprises pharmaceutiques, les gouvernements, le monde universitaire, les secteurs privé et philanthropique pour découvrir, développer et commercialiser de nouveaux traitements ou réorganiser les moyens de production. »
De son côté, la Fédération internationale des associations pharmaceutiques et fabricants (IFPMA) a réagi après la publication de cet article. Par la voix de son directeur général, Thomas Cueni, elle affirme que « dès le début de la pandémie, l’industrie pharmaceutique a pris conscience de l’ampleur de la crise et a très vite fait passer la santé publique avant les bénéfices privés. L’industrie pharmaceutique a publiquement souligné son engagement à garantir un accès rapide, équitable et abordable aux thérapies et vaccins pour la Covid-19 une fois approuvés. »
L’IFPMA renvoie à son site internet, qui recense les initiatives prises par l’industrieLien externe dans le contexte du coronavirus.
Réactivité exceptionnelle des HUG
Il n’en reste pas moins que plus de la moitié des essais (54%) sont conduits par des institutions publiques. Environ 15% émanent d’oeuvres philanthropiques et d’universités privées. Une part à peu près équivalente provient d’organismes purement privés (pharma, cliniques privées, organisations de soins intégrés…) et de partenariats.
Alexandra Calmy, spécialiste des maladies infectieuses aux Hôpitaux Universitaires de Genève (HUG), conduit actuellement un essai pour tester l’effet prophylactique contre la Covid-19 de l’hydroxycloroquine et de deux médicaments utilisés originellement pour traiter les malades du sida. Elle explique que la mise en place de cette étude a été exceptionnelle. « L’effort a été incroyablement rapide et intense, avec un soutien décisif de l’hôpital et de la fondation des HUG », notamment pour mettre à disposition, dans l’urgence, le personnel nécessaire.
Pas d’intérêt « marketing »
Du côté des HUG, tout le monde a compris « l’urgence de la situation ». Mais comment se fait-il que ce soit une institution publique qui teste des produits habituellement commercialisés par les groupes pharmaceutiques Sanofi, Novartis et Abbvie? La réponse de la chercheuse est claire: « ces molécules sont déjà sur le marché depuis longtemps, elles ne présentent plus d’intérêt marketing ».
La plupart des traitements testés sont déjà utilisés pour d’autres affections. Les chercheurs pensent qu’ils pourraient être efficaces contre la coronavirus. La protection par des brevets de ces anciens médicaments est limitée, voire échue. Ils sont donc moins profitables, ce qui expliquerait pourquoi des organismes publics mènent l’essentiel des recherches sur ces produits de l’industrie.
Les médicaments récents présentent plus d’intérêt financier pour les groupes pharmaceutiques. Seulement, l’industrie a largement désinvesti le champ des maladies virales, jugé trop risqué financièrement. Les candidats sont donc peu nombreux. A noter que pour ceux-ci aussi, universités et hôpitaux ont largement participé à l’effort d’investigation.
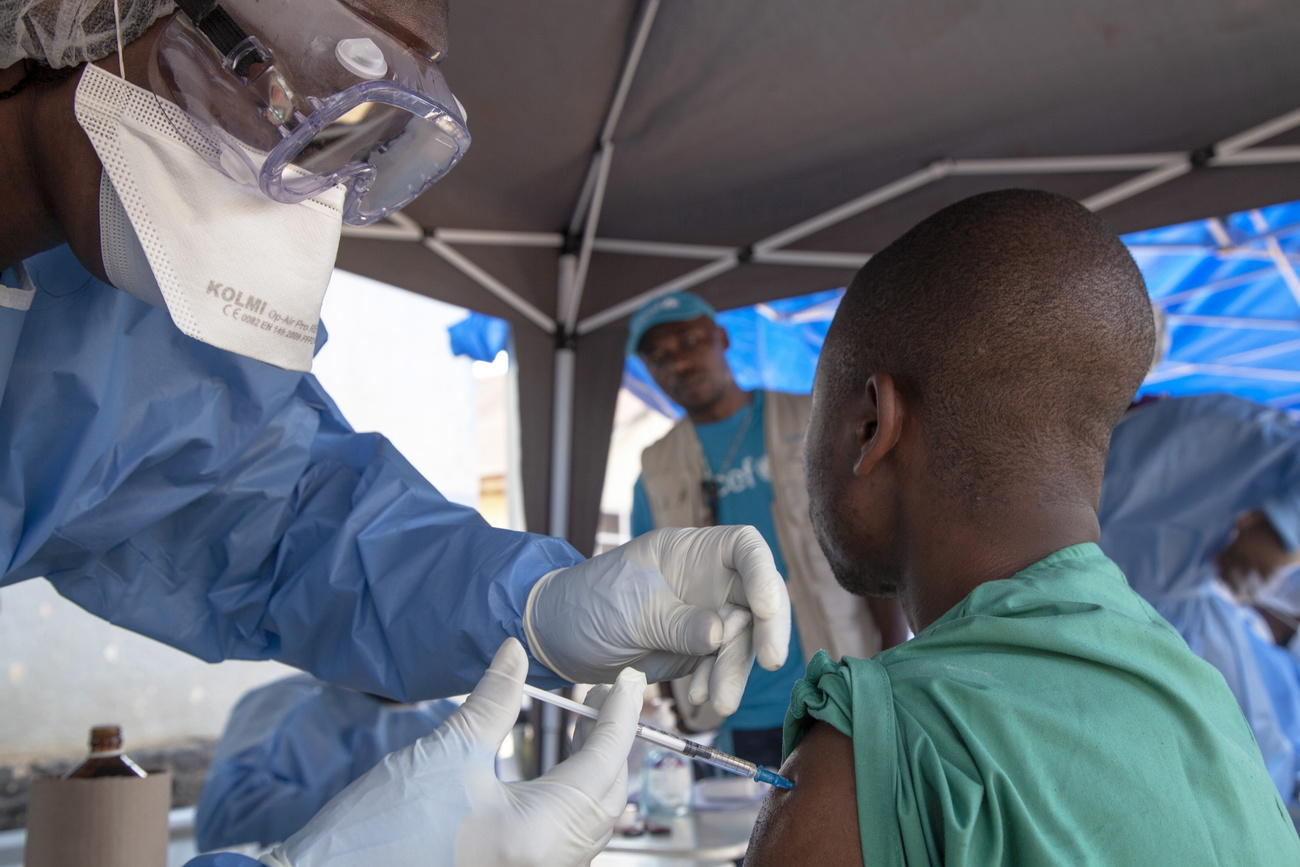
Plus
Pourquoi les géants de la pharma boudent le coronavirus
Coûts et accessibilité incertains
Reste à savoir sur quelle manne économique ces recherches déboucheront et qui en bénéficiera. Les recherches universitaires et publiques contribuent très fréquemment au développement de nouveaux médicaments par l’industrie. Dans le cas de la Covid-19, ils auront, en plus, été largement expérimentés via ces ressources. Malgré cela, ces contributions ne suffisent pas à garantir des tarifs supportables pour tout le monde.
Au contraire, quelques signaux contradictoires ont émané de l’industrie. Gilead a par exemple tenté d’augmenter le potentiel commercial du Remdesivir en demandant le statut de traitement orphelin. Face au tollé, l’entreprise a reculé. Elle a ensuite accepté de lâcher une partie de ses droits pour permettre une production à bas prix dans les pays les plus pauvres. Abbvie a renoncé à ses droits sur un traitement contre le sida, « un geste rare, bien que tardif, que l’on peut souligner », selon la professeure Alexandra Calmy.
Néanmoins, ces décisions relèvent largement du bon vouloir des sociétés pharmaceutiques. Elles portaient sur des traitements en fin de vie commerciale ou dont l’efficacité avait été relativisée par les premières études.
Pouvoirs publics inoffensifs
« Il faut lier les financements à des conditions qui assurent que ces découvertes demeurent un bien public global, partout dans le monde », estime Ellen ‘t Hoen, ce qui n’est pas le cas actuellement. Pour cette connaisseuse des questions juridiques dans le monde de la pharma, il est évident que « les précautions et mesures ne sont pas prises par les pouvoirs publics pour s’assurer que le fruit de ses recherches sera accessible à tous. »
L’accessibilité, le prix et le poids sur les systèmes de santé d’un traitement efficace, s’il devait être trouvé, pourrait susciter de sérieux débats. Ce pourrait être le cas, y compris en Suisse, où un traitement à large échelle ne manquerait pas d’alourdir les primes d’assurance-maladie en cas de traitement ambulatoire et les contribuables pour ce qui est des soins hospitaliers.
Essais cliniques sur la chloroquine: les précisions de la professeure Alexandra Calmy dans le 19h30 de la RTS:

En conformité avec les normes du JTI
Plus: SWI swissinfo.ch certifiée par la Journalism Trust Initiative





Vous pouvez trouver un aperçu des conversations en cours avec nos journalistes ici. Rejoignez-nous !
Si vous souhaitez entamer une conversation sur un sujet abordé dans cet article ou si vous voulez signaler des erreurs factuelles, envoyez-nous un courriel à french@swissinfo.ch.