Was wurde aus dem teuersten Medikament der Welt?

Stolze 2,1 Millionen Dollar kostete das Medikament, als es vor fünf Jahren auf den Markt kam: Zolgensma ist eine einmalige Behandlung für Säuglinge, die mit einer seltenen und oft tödlichen Erbkrankheit geboren wurden. Doch der Schweizer Hersteller Novartis gerät zunehmend unter Druck, weil die jährlichen Umsätze sinken und neue Märkte schwer zu erschliessen sind.
Als Novartis-Konzernchef Vas Narasimhan im Januar die Jahresergebnisse 2023 des Unternehmens vorstellte, wurde Zolgensma nicht einmal erwähnt.
Zolgensma wurde 2019 mit viel Tamtam eingeführt, als erste Gentherapie zur Behandlung von spinaler Muskelatrophie (SMA). SMA ist eine seltene neuromuskuläre Erkrankung und eine der weltweit häufigsten genetischen Ursachen für das Sterben von Kindern.
Die einmalige Infusion wurde ursprünglich als potenzielles Heilmittel für SMA angepriesen – und als einer der sechs wichtigsten Wachstumstreiber des Schweizer Pharmariesen mit einem Umsatzpotenzial von mehreren Milliarden Dollar.
Die Konsensschätzung der Analystinnen und Analysten lag damals bei 1,9 Milliarden Dollar (1,7 Milliarden Franken) Umsatz pro Jahr, die Prognose einer InvestmentbankExterner Link sogar bei 2,8 Milliarden Dollar.
Im Jahr 2021 stieg der Umsatz mit Zolgensma um 46 Prozent auf 1,35 Milliarden Dollar, nachdem die Europäische Arzneimittelagentur 2020 eine bedingte Zulassung für die Behandlung erteilt hatte.
Zolgensma, der Markenname des Medikaments Onasemnogen abeparvovec, konnte diese Dynamik jedoch nicht aufrechterhalten. Im Jahr 2022 stieg der weltweite Umsatz in Dollar nur noch um 1%, 2023 sank er um 11% auf 1,21 Mrd. Dollar.
In den USA, dem grössten Einzelmarkt des Unternehmens, ging der Umsatz im vergangenen Jahr um 14% auf 372 Mio. Dollar zurück.
Für Matthias Bünte, Managing Partner bei der Unternehmensberatung Roland Berger in Zürich und spezialisiert auf Marktzugangs- und Wachstumsstrategien für Pharmaunternehmen, ist das keine Überraschung.
«Nach einer anfänglichen Wachstumsphase in den wichtigsten Märkten werden die Umsätze durch die Geburtenrate der in Frage kommenden SMA-Patientinnen und Patienten begrenzt», sagt er.
«Das ist bei einer einmaligen Behandlung zu erwarten. Es ist nicht vergleichbar mit einer chronischen Behandlung, die eine kontinuierliche Einnahmequelle bietet, die mit jeder neuen betroffenen Person wächst.»
Die rückläufigen Zolgensma-Umsätze und die abnehmende Bedeutung des Medikaments in der Gewinnberichterstattung von Novartis sind weit entfernt von den optimistischen Aussichten, die das Unternehmen versprach, als es den Entwickler des Medikaments, das an der Nasdaq notierte Startup «AveXis», im Jahr 2018 für 8,7 Milliarden US-Dollar kaufte, um sein Gentherapiegeschäft zu stärken.
Einer der Hauptgründe für die stagnierenden Umsätze ist, dass «etablierte Märkte [wie die USA] jetzt hauptsächlich inzidente statt prävalente Patientinnen und Patienten behandeln», so eine Novartis-Sprecherin in einer schriftlichen Stellungnahme gegenüber SWI.
Mit anderen Worten: Das Unternehmen hat bereits alle in Frage kommenden SMA-Patientinnen und Patienten erreicht und kann sich in Zukunft nur noch auf neu diagnostizierte Betroffene verlassen, um das Umsatzwachstum des Medikaments in diesen Märkten zu unterstützen.
Für Novartis ist es schwierig, in Märkte ausserhalb der relativ wohlhabenden Länder in Nordamerika und Europa vorzudringen, da Regierungen mit knappen Gesundheitsbudgets in Frage stellen, ob das Medikament wirksam genug ist, um seinen Preis zu rechtfertigen.
Mehr
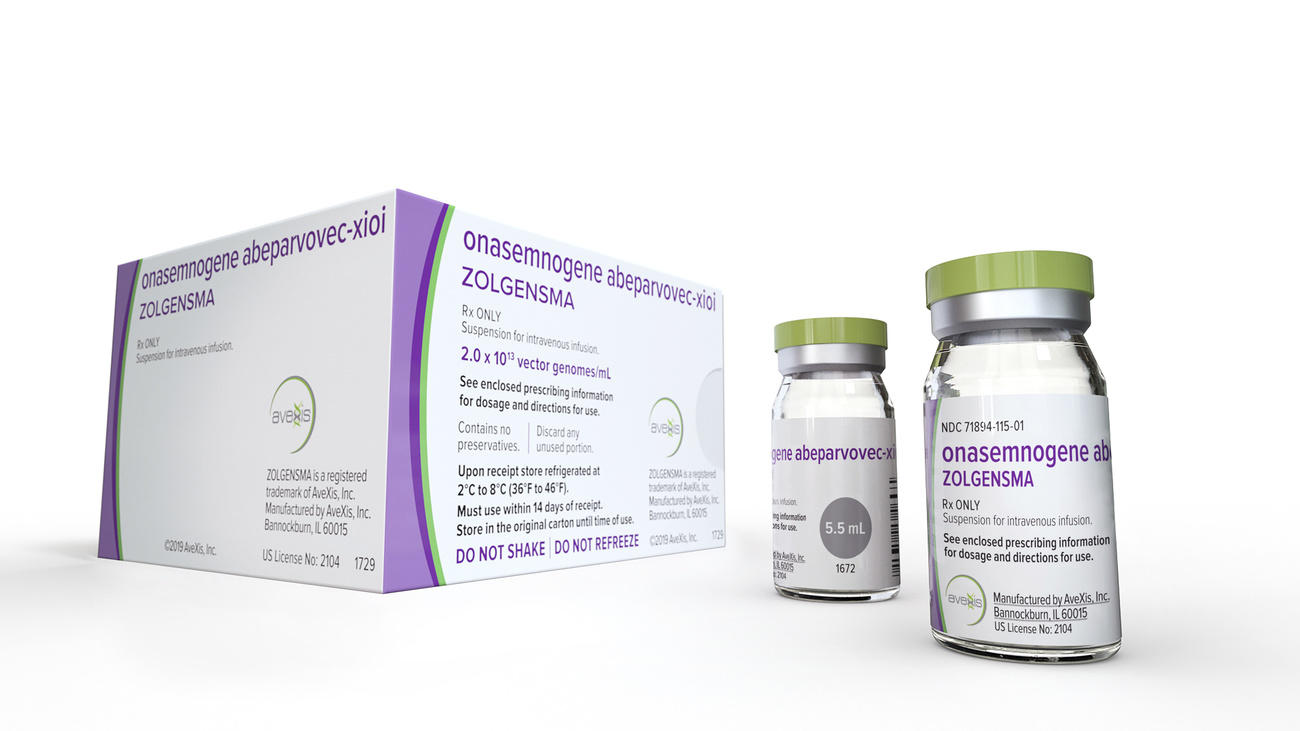
Wie kann ein Medikament 2,1 Mio. Franken kosten?
Die US-amerikanische Food and Drug Administration (FDA), die weltweit als Goldstandard für die Zulassung von Arzneimitteln gilt, gab 2019 als erste Behörde grünes Licht für Zolgensma, das von Novartis zu einem Preis von 2,1 Millionen US-Dollar angeboten wurde.
Obwohl Zolgensma bis Januar 2024 in 51 Ländern zugelassen ist und mehr als 3700 Patientinnen und Patienten behandelt wurden, bieten nur 35 Länder eine Kostenerstattung an.
Das bedeutet, dass sich viele von SMA betroffene Familien ein potenziell lebensrettendes Medikament nicht leisten können oder auf Crowdfunding angewiesen sind.
Wie Novartis den Preis rechtfertigt
SMA betrifft weltweit etwa eines von 10’000 Kindern, in den USA sind das etwa 300 Neugeborene pro Jahr. Sie wird durch eine Mutation im Gen SMN1 verursacht, die verhindert, dass die Zellen genügend vom Protein SMN produzieren, das wichtige Signale an die Muskeln sendet. Dieser Mangel beeinträchtigt die Motoneuronen, wodurch die Muskeln geschwächt werden.
Unbehandelt können Kinder mit der schwersten Form von SMA ihren Kopf oder ihre Beine nie heben und haben Schwierigkeiten beim Schlucken und Atmen.
Die meisten von ihnen sterben im Alter von zwei Jahren, oft aufgrund von Atemproblemen. SMA-Symptome können auch bei Erwachsenen auftreten, sind aber weniger schwerwiegend.
SMA wird durch das Fehlen oder die Mutation des Gens SMN1 verursacht, das die Herstellung des Proteins SMN (Survival Motor Neuron) steuert. Das bedeutet, dass wenig oder gar kein SMN-Protein produziert wird, wodurch die Motoneuronen erkranken und absterben, was zu fortschreitendem Muskelschwund führt.
Alle Menschen mit SMA haben mindestens ein «Ersatzgen», das als SMN2 bezeichnet wird. Patientinnen und Patienten mit mehr Kopien dieses Gens neigen zu einer milderen Form der SMA und entwickeln die Symptome erst später im Leben.
SMA wird in vier klinische Typen eingeteilt, die sich nach dem Alter des Ausbruchs und der motorischen Funktion richten. Typ 1 (nicht in der Lage, selbständig zu sitzen und tritt in der Regel bei Säuglingen unter 6 Monaten auf), Typ 2 (in der Lage, selbständig zu sitzen, aber nicht zu gehen), Typ 3 (selbständiges Gehen) und Typ 4 (selbständiges Gehen und Ausbruch der Krankheit im Erwachsenenalter).
Die häufigste Form der SMA, an der 45% bis 60% der Betroffenen leiden, ist Typ 1. Diese Kinder überleben in der Regel nicht länger als zwei Jahre, wenn sie nicht maschinell beatmet und ernährt werden.
Es ist medizinisch erwiesen, dass die Betroffenen umso besser auf eine Behandlung ansprechen, je früher sie diese erhalten. In vielen Ländern wird SMA jedoch nicht im Neugeborenen-Screening erfasst.
Die Entwicklung von Medikamenten zur Behandlung seltener Krankheiten wie SMA kann Jahre dauern und Milliarden von Dollar kosten. Die Unternehmen verkaufen sie schliesslich zu hohen Preisen, um ihre Investitionen zu amortisieren und die geringen Verkaufszahlen auszugleichen.
Novartis rechtfertigte den Preis von Zolgensma damit, dass es sich um eine einmalige Infusion handle, die auf die genetische Ursache der Krankheit abziele.
Indem das Medikament ein defektes Gen durch ein funktionierendes ersetze, würde es nicht nur Leben retten, sondern auch Familien und nationalen Gesundheitssystemen eine lebenslange, kostspielige Behandlung ersparen.
Bevor die Gentherapie auf den Markt kam, war die einzige andere verfügbare Behandlung für SMA Nusinersen, das 2016 von der US-Firma Biogen unter dem Namen Spinraza auf den Markt gebracht wurde und 300’000 bis 500’000 Dollar pro Jahr über die gesamte Lebenszeit einer betroffenen Person kostet.
Bei einer Einnahme über zehn Jahre würde das Medikament, das dreimal jährlich als Injektion in die Wirbelsäule verabreicht werden muss, den Listenpreis von Zolgensma von 2,1 Millionen Dollar bei weitem übersteigen.
Novartis hat nicht erklärt, wie es den Preis für Zolgensma berechnet hat, und unabhängige Bewertungen kommen zu sehr unterschiedlichen SchätzungenExterner Link, wie viel das Medikament kosten sollte – von 710’000 Dollar bis zu mehr als den verlangten 2,1 Millionen Dollar.
Die Tatsache, dass zum Zeitpunkt der Preisfestsetzung nur so wenige Patientinnen und Patienten das Medikament erhalten hatten, warf auch Fragen über seinen tatsächlichen Wert auf.
Wie viele Behandlungen für lebensbedrohliche seltene Krankheiten erhielt Zolgensma in den USA, Europa und Japan grünes Licht im Rahmen eines beschleunigten ZulassungsverfahrensExterner Link, was den Patientinnen und Patienten einen schnelleren Zugang zu einem potenziell lebensrettenden Medikament ermöglicht.
Die FDA stützte ihren Entscheid auf eine abgeschlossene Studie im Frühstadium und eine laufende Studie im Spätstadium mit insgesamt weniger als 40 Patientinnen und Patienten.
Die Mehrheit der mit Zolgensma behandelten Kinder überlebte, konnte selbstständig atmen und erreichte zwei Jahre nach der Einnahme des Medikaments Meilensteine wie die Fähigkeit, ohne Hilfe aufzustehen.
Die Fortschritte waren jedoch sehr unterschiedlich, und bei einigen Kindern traten schwere Nebenwirkungen auf, darunter Leberprobleme. Der kurze Zeitrahmen bedeutete auch, dass es keine Daten darüber gab, wie lange die Vorteile des Medikaments anhalten würden. Ausserdem gab es nur wenige Studienteilnehmende von ausserhalb der USA.
Die USA und einige reiche Länder beschränkten Zolgensma auf die jüngsten Patientinnen und Patienten (unter zwei Jahren) mit der schwersten Form von SMA, für die es die besten Belege für Sicherheit und Wirksamkeit gab.
Die Europäische Arzneimittelagentur hat das Medikament für Kinder mit einem Gewicht von bis zu 21 Kilogramm zugelassen, was Kleinkinder von bis zu fünf Jahren einschliessen kann. Aber viele Mitgliedstaaten erstatten nur die Behandlung von Kindern unter sechs Monaten.
Die Hürde des hohen Preises
Da das Wachstumspotenzial in den etablierten Märkten begrenzt ist, misst Novartis der Ausweitung der geografischen Reichweite von Zolgensma entscheidende Bedeutung zu.
Doch angesichts konkurrierender Gesundheitsanforderungen und begrenzter Budgets wollen viele Länder mit mittlerem Lohnniveau mehr Beweise dafür, dass das Medikament den hohen Preis rechtfertigt.
«Bei seltenen Krankheiten besteht die Herausforderung darin, dass der Zugang zu den Medikamenten schnell erfolgen muss. Aber gleichzeitig sind die Preise für diese Medikamente extrem hoch und es bestehen viele Unsicherheiten. Manchmal kennt man den tatsächlichen klinischen Nutzen nicht», sagt Vera Pepe, Forscherin im Bereich der öffentlichen Gesundheit und Mitverfasserin eines Artikels über den Zugang zu Zolgensma in BrasilienExterner Link.
«Aber das belastet die Gesellschaft mit der Finanzierung extrem teurer Medikamente mit begrenzten Nachweisen für den klinischen Nutzen und grossen Unsicherheiten, mit enormen Opportunitätskosten, vor allem in universellen Gesundheitssystemen wie dem unseren.»
Die brasilianische Regierung und Novartis verhandelten mehr als zwei Jahre lang über den Preis und die Bedingungen für das Medikament und einigten sich schliesslich Ende 2022.
Das Unternehmen erklärte sich bereit, die Behandlung für bis zu 250 Babys zu einem Preis von 1,1 Millionen US-Dollar pro Infusion bereitzustellen und verpflichtete sich dazu, in Brasilien Studien über die langfristigen Auswirkungen der Behandlung durchzuführen.
Andere Länder, darunter die Türkei, lehnen das Medikament jedoch weiterhin mit der Begründung ab, es gebe nicht genügend Beweise für seine Sicherheit und Wirksamkeit.
«Unternehmen können nicht mehr einfach ein zwei Millionen Dollar teures Medikament auf den Markt bringen und erwarten, dass die Regierungen dafür bezahlen», sagt Girisha Fernando, Chef von Lyfegen, einem globalen Anbieter von Lösungen für die Preisgestaltung und das Rabattmanagement. «Sie müssen mehr bieten als das.»
Novartis sucht nach Wegen, Zolgensma auch in Ländern mit mittlerem Lohnniveau zugänglich zu machen, und bietet Krankenkassen und nationalen Gesundheitsbehörden Rabatte, Ratenzahlungspläne und Risikoteilungsvereinbarungen an, bei denen die Bezahlung von zuvor vereinbarten Ergebnissen abhängt.
Im vergangenen Jahr unterzeichnete das Unternehmen einen solchen Vertrag mit der argentinischen nationalen Krankenkasse, um Zolgensma für 1,3 Millionen Dollar zur Verfügung zu stellen.
Die Zahlung erfolgt nur, wenn «die bei den Patientinnen und Patienten beobachteten Ergebnisse mit denen übereinstimmen, die aufgrund der verfügbaren wissenschaftlichen Daten zu erwarten sind», heisst es in einer Kopie des Vertrags in der Lyfegen-Bibliothek der VereinbarungenExterner Link.
Für die Familien von Kindern mit SMA ist das Warten auf eine Behandlung eine Qual. Je länger die Kinder ohne Behandlung auskommen müssen, desto mehr verschlechtert sich ihr Zustand und kann auch mit Zolgensma nicht mehr rückgängig gemacht werden.
«Es ist sehr belastend für die Eltern, weil Leben verloren gehen», sagt Vanina Sanchez, Präsidentin der SMA-Vereinigung FAME Argentina, deren Sohn an SMA erkrankt ist.
«Wenn es sich um Babys mit Typ 1 handelt, der schwersten Form der Krankheit, haben sie wirklich keine Zeit zu verlieren», sagt sie.
Daten-Dilemma
Novartis wurde zum Teil durch die Ergebnisse weiterer klinischer Studien und so genannter «Real-World»-Daten von Gesundheitsdienstleistern aus aller WeltExterner Link unterstützt, die positive Ergebnisse für viele Patientinnen und Patienten zeigten, welche die Therapie erhalten hatten.
Im März 2023 zeigten eigene Studien von NovartisExterner Link, dass Kinder, die als Säuglinge Zolgensma erhalten hatten, sieben Jahre nach der Einnahme des Medikaments wichtige motorische Meilensteine wie das Aufstehen beibehielten und in der Lage waren, ohne Hilfe zu atmen.
Ältere Kinder mit milderen Formen der Krankheit, die eine neuere Version des Medikaments in höherer Dosierung erhalten hatten, zeigten ebenfalls Verbesserungen.
Mehr
Mit Hightech gegen die Kostenspirale bei Medikamenten
Einige machten jedoch keine Fortschritte mehr, und 24 der 81 Kinder in den Studien wurden anschliessend mit anderen SMA-Medikamenten behandelt.
Andere Studien, darunter eine in der SchweizExterner Link, an der neun Kinder teilnahmen, unterstreichen die grosse Bandbreite möglicher Ergebnisse.
Die wachsende Zahl von Studien- und Behandlungsergebnissen zeigt, dass sich der anfängliche Hype um Zolgensma als alleiniges Heilmittel für SMA-Patientinnen und Patienten in der Realität nicht bestätigt hat.
«Eltern erwarten, dass ihr Kind geheilt wird, weil die Gentherapie anfangs so beworben wurde. Das hat falsche Erwartungen geweckt für eine Krankheit, die sehr komplex ist und noch immer nicht vollständig verstanden wird», sagt Nicole Gusset. Sie ist Leiterin der Betroffenenorganisationen SMA Europa und SMA Schweiz und Mutter einer an SMA erkrankten Tochter.
«Heilung ist ein grosses Wort und sollte sparsam verwendet werden. Eine Stabilisierung des Krankheitsverlaufs oder die Abwesenheit von sichtbaren Symptomen sind enorme Erfolge, aber sie bedeuten nicht automatisch, dass eine Krankheit geheilt ist», sagt sie gegenüber SWI swissinfo.ch.
Novartis sieht sich auch einem grösseren Druck ausgesetzt, da andere Medikamente zur Behandlung von SMA auf den Markt kommen.
Im Jahr 2020 erteilte die US-amerikanische Arzneimittelbehörde FDA dem Schweizer Konkurrenten Roche die Zulassung für Ridisplam für ältere Kinder und Erwachsene mit SMA, das unter dem Namen Evrysdi verkauft wird.
Die Zulassung wurde kürzlich auf Säuglinge unter zwei Monaten ausgeweitet, was das Medikament zu einem direkten Konkurrenten von Zolgensma macht.
Evrysdi ist in Form von Tabletten und Sirup erhältlich, wodurch es einfacher zu verabreichen ist als eine Gentherapie, und kostet je nach Gewicht des Kindes zwischen 100’000 und 350’000 Dollar pro Jahr.
Evrysdi ist in mehr als 100 Ländern zugelassen und wird weltweit zur Behandlung von mehr als 11’000 SMA-Betroffenen eingesetzt.
«Alle Behandlungen sind in der Lage, den Krankheitsverlauf zu stabilisieren», sagt Gusset. «Was wir noch nicht wissen, ist, welche Behandlung bei welcher Bevölkerungsgruppe oder bei welchen Personen am besten wirkt.»
Fachleute des Schweizer Registers für seltene Krankheiten, das an der Universität Bern eingerichtet wurde, stimmen dem zu und erklären in einer E-Mail an SWI swissinfo.ch, es gebe insgesamt nicht genügend Beweise, um zu bestimmen, welche der drei Therapien (Spinraza, Zolgensma und Evrysdi) überlegen sei.
Der angemessene Preis
Andere Entwickler von Gentherapien, die Milliarden in neue Medikamente investieren, beobachten genau, wie der Schweizer Pharmariese mit diesem Gegenwind umgeht.
Bei den US-Behörden sind mehr als 1500 laufende klinische StudienExterner Link für Zell- und Gentherapien registriert.
Und im vergangenen Jahr hat die FDA fünf zugelassen, darunter zwei für die Sichelzellkrankheit, deren Listenpreise höher sind als die von Zolgensma – 2,2 und 3,1 Millionen Dollar.
Im März stellte Orchard Therapeutics in den USA mit 4,25 Millionen Dollar einen neuen Rekord für Lenmeldy (auch Libmeldy genannt) auf, eine Gentherapie für metachromatische Leukodystrophie.
Das ist eine extrem seltene genetische Erkrankung, die das zentrale Nervensystem von Säuglingen befällt und woran jedes Jahr in den USA etwa 40 Neugeborene erkranken.
«Die Regierungen stehen unter Druck, den Patientinnen und Patienten neue Medikamente zur Verfügung zu stellen», sagt Kerstin Noëlle Vokinger, Expertin für Arzneimittelpreise und Professorin an der Rechts- und Medizinischen Fakultät der Universität Zürich.
«Das ist verständlich, denn Patientinnen und Patienten mit seltenen oder lebensbedrohlichen Krankheiten brauchen eine Behandlung. Aber wie soll man den Preis eines Medikaments aushandeln, wenn man dessen tatsächlichen therapeutischen Wert nicht kennt?»

Mehr
Was ist ein fairer Preis für ein Medikament?
Einige Gentherapien sind aufgrund von Preisstreitigkeiten bereits vom Markt verschwunden. Mindestens sieben von 25 zugelassenen Zell- und Gentherapien wurden von den Arzneimittelherstellern in Europa vom Markt genommenExterner Link.
Am bekanntesten ist Zynteglo, ein Medikament gegen die Blutkrankheit Beta-Thalassämie. Sein Hersteller, die US-Firma Bluebird Bio, hat nach mehreren Streitigkeiten über den Preis des Medikaments ihre Aktivitäten in der EU eingestellt.
«Eine grosse Sorge ist, dass Medikamente vom Markt genommen werden, weil sie zu teuer sind oder sich nicht verkaufen», sagt Kelly Ormond, Genetik-Beraterin und -Forscherin am Health Ethics and Policy Lab der ETH Zürich.
«Wenn wir nutzen wollen, was Gentherapien und andere Präzisionsmedizin für Versprechungen bringen, müssen wir klären, wie wir dafür bezahlen.»
Editiert von Nerys Avery, Übertragung aus dem Englischen: Christian Raaflaub
Mehr

In Übereinstimmung mit den JTI-Standards











Einen Überblick über die laufenden Debatten mit unseren Journalisten finden Sie hier. Machen Sie mit!
Wenn Sie eine Debatte über ein in diesem Artikel angesprochenes Thema beginnen oder sachliche Fehler melden möchten, senden Sie uns bitte eine E-Mail an german@swissinfo.ch