
Un arma contra las superbacterias del Rin
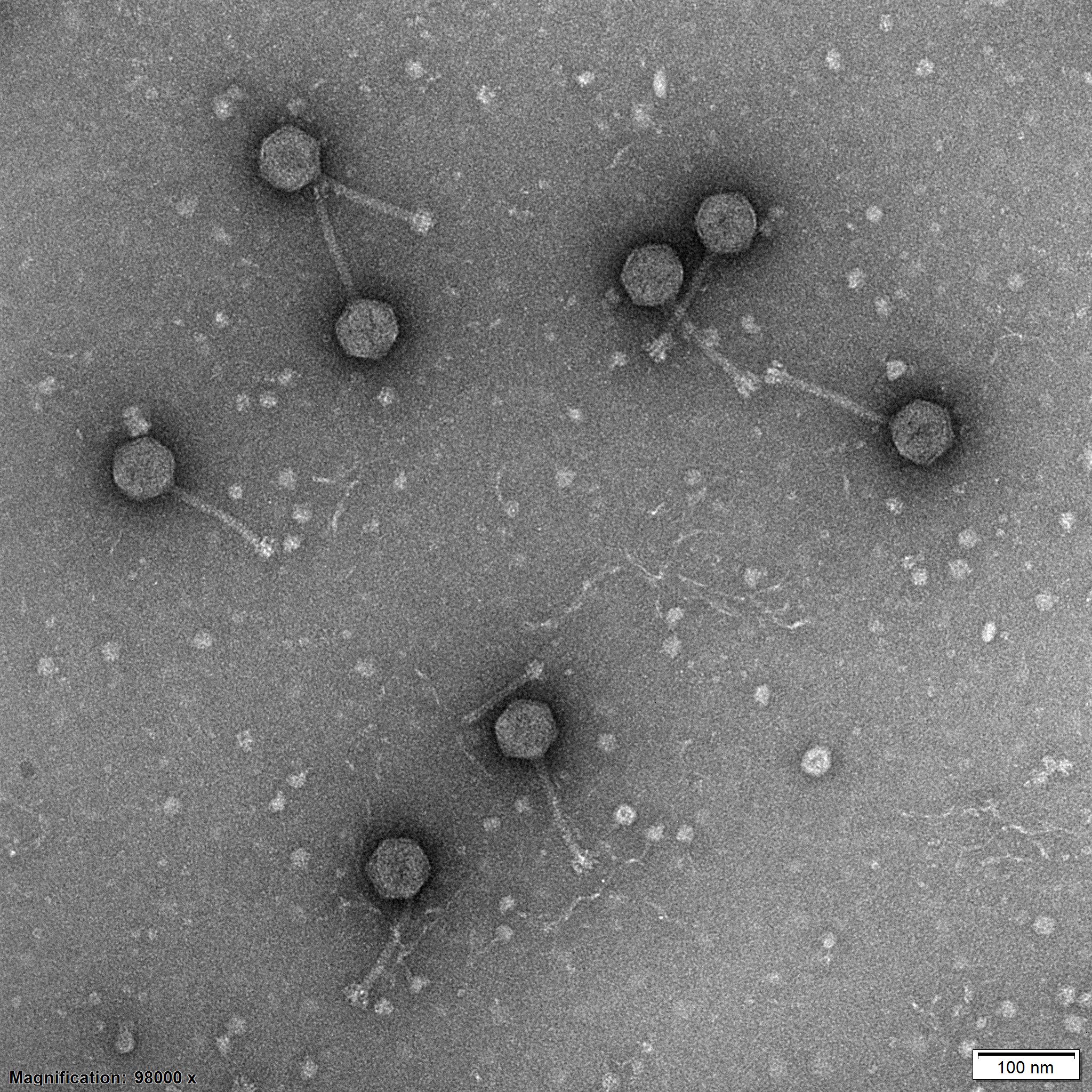
Una de las mayores amenazas para la salud de las personas son las bacterias resistentes a los antibióticos. Una colección única de virus bacteriófagos aislados en Suiza está ayudando a personal investigador de todo el mundo a desarrollar nuevas terapias contra infecciones que de otro modo son incurables.
Después de haber salido de la pandemia de COVID-19 hablar de virus beneficiosos puede parecer una contradicción. Sin embargo, no todos los virus son perjudiciales para nuestra salud. Aquellos que infectan bacterias —llamados bacteriófagos o de manera abreviada fagos— pueden resultar muy útiles y salvar vidas, dice el microbiólogo Alexander Harms. No obstante, todavía se sabe muy poco sobre ellos. “Estudiarlos es como explorar la cara oculta de la Luna”, afirma.
Se trata de una misión hacia lo desconocido que este investigador alemán emprendió en 2019 junto a un grupo de estudiantes de secundaria. Durante un curso de verano en Basilea, recogieron y caracterizaron muestras de bacteriófagos presentes en la naturaleza. Ahora estos virus se han convertido en un importante recurso para institutos de investigación de todo el mundo y podrían contribuir en el futuro a tratar infecciones bacterianas.

«Asesinos» de bacterias
Los fagos —al igual que todos los virus— no pueden duplicarse por sí mismos, sino que tienen que aprovechar los sistemas metabólicos de las bacterias a las que infectan. Tras duplicarse —mediante la ruptura de la membrana celular (lisis celular)—, los fagos inducen la muerte de quien los acoge.
Se encuentran entre las entidades biológicas más abundantes y extendidas de la Tierra. Se cuentan por miles de millones de millones y están prácticamente en todos los ecosistemas del planeta: desde el suelo de los bosques hasta la superficie de los océanos. Desempeñan un papel fundamental en la ecología y en el ciclo del carbono. Gracias a su actividad lítica, por ejemplo, contribuyen a difundir los nutrientes que contienen las bacterias marinas.
“Están entre las fuerzas motrices de nuestro planeta”, indica Alexander Harms, colaborador hasta el año pasado del Biozentrum de la Universidad de Basilea —instituto especializado en investigación biomédica molecular y básica— y del Instituto de Alimentación, Nutrición y Salud de la Escuela Politécnica Federal de Zúrich, en la actualidad.
Los fagos también están presentes en nuestro organismo. No atacan a las células humanas, pero pueden influir en la composición de la población bacteriana. Con todo, su impacto en la microbiota intestinal todavía se ha estudiado poco.
>> Esta animación (en inglés) ilustra el ciclo de vida de un bacteriófago:
Según Harms, la capacidad de infectar las bacterias de manera selectiva —un fago solo reconoce una determinada especie de bacteria y a menudo solo determinadas cepas de esa especie— convierte los fagos en herramientas de investigación sumamente interesantes. Pueden destruir los gérmenes patógenos que han contaminado los alimentos —en el caso de la salmonela, por ejemplo— o pueden utilizarse para tratar infecciones bacterianas del aparato urinario o respiratorio.
Y es precisamente el interés por los fagos que atacan a las llamadas bacterias “latentes” —responsables de infecciones crónicas— lo que ha llevado a Alexander Harms a tomar los tubos de ensayo e ir a buscar bacteriófagos en la naturaleza.
Nuevos bacteriófagos en las aguas del Rin
Como parte del curso de verano Basel Summer Science Academy, organizado por Biozentrum, en el verano de 2019 Alexander Harms y un grupo de estudiantes de secundaria recogieron muestras de agua y del suelo en el río Rin, estanques, plantas de compostaje y estaciones depuradoras en la región de Basilea. “No sabíamos lo que nos esperaba”, recuerda Harms.

El equipo de Harms en el laboratorio aisló un gran número de bacteriófagos que infectan la Escherichia coli (una bacteria intestinal muy común y por lo general inofensiva, pero que en algunos casos puede causar enfermedades graves) y describió sus características al detalle. El resultado —una colección de 70 tipos de fagos— se publicó dos años después en la revista científica PLOS Biology.
La colección confirma que grupos de fagos similares desempeñan el mismo papel y la misma función en todo el mundo, desde China hasta los Estados Unidos. “Esto me ha sorprendido mucho”, señala Alexander Harms.
Aunque es, sobre todo, la primera representación de la diversidad de fagos que infectan la Escherichia coli. En el mundo hay colecciones más grandes —compuestas por hasta cientos de fagos— pero ninguna los caracteriza de manera tan sistemática como la de Basilea, sostiene el investigador.
La colección también es útil para quienes investigan en el extranjero y desean utilizar fagos —como alternativa a los antibióticos— para tratar infecciones bacterianas. Han demostrado ser prometedores, en particular, en la lucha contra las bacterias que infectan las úlceras y las heridas crónicas en personas diabéticas que a menudo conducen a la amputación.

El renacimiento de los fagos en medicina
La idea de utilizar los fagos como terapia médica —administrándolos por vía intravenosa o como aerosoles— surgió ya en las primeras décadas del siglo XX, especialmente en la antigua Unión Soviética. Los fagos se utilizaron durante la Segunda Guerra Mundial para tratar a los soldados que sufrían disentería y otras infecciones bacterianas. De todas formas, con la llegada y difusión de los antibióticos —la penicilina se descubrió en 1929—, la investigación sobre estos virus beneficiosos quedó relegada a un segundo plano, al menos en Occidente.
Pero —con el aumento en todo el mundo de la resistencia a los antibióticos—infecciones como la neumonía o la tuberculosis, por citar algunas, son más difíciles de combatir. Según un estudio publicado en 2022, cada año en el mundo mueren más de 1,2 millones de personas por la resistencia a los antimicrobianos; más que por el VIH o la malaria. Para el año 2050, las muertes podrían aumentar a 10 millones anuales.
La Organización Mundial de la Salud (OMS) considera que en la actualidad la resistencia a los antibióticos es una amenazagrave para la seguridad sanitaria mundial; y los países occidentales también han intensificado la investigación sobre terapias con fagos, que casi no tienen efectos secundarios y conllevan riesgos limitados.
Los mismos requisitos que otros medicamentos
Harms dice que, aunque se habla mucho de ello, el uso terapéutico de los bacteriófagos aún no está tan extendido. El proceso de identificar la bacteria responsable de una infección y seleccionar el fago adecuado para matarla puede ser complejo y costoso. Los fagos pueden estar sujetos a la reacción inmunitaria del organismo o, como los antibióticos, inducir resistencia cuando se administran repetidamente.
Además, a diferencia de un antibiótico con propiedades bien definidas y estables —y por tanto replicables—, un bacteriófago es más complejo y puede sufrir mutaciones. Una característica que dificulta la autorización para su uso terapéutico. “Si se utilizan con fines terapéuticos, los preparados a base de fagos deben cumplir los mismos requisitos que el resto de los medicamentos”, explica Lukas Jaggi, portavoz de la Agencia Suiza de Productos Terapéuticos Swissmedic.
Hasta la fecha, en Suiza no se ha autorizado ningún preparado de este tipo. Sin embargo, en 2015 se puso en marcha un estudio clínico y no puede descartarse que profesionales de la medicina hayan utilizado fagos procedentes del extranjero para tratar infecciones en casos aislados, señala Jaggi.
Del Rin a Australia
Alexander Harm tiene la esperanza de que la colección de fagos de Basilea pueda estimular aún más la búsqueda de terapias eficaces. Y no solo en el ámbito humano. “Los fagos podrían resultar útiles en la lucha contra las bacterias que destruyen plantaciones”, afirma. Preparados a base de fagos podrían rociarse, por ejemplo, en los olivares afectados por la Xylella fastidiosa —una bacteria responsable de la muerte de miles de plantas en Apulia— o en las plantaciones de manzanas y peras de Suiza afectadas por el “fuego bacteriano” (Erwinia amylovora).
Hasta ahora más de 40 laboratorios de todo el mundo han solicitado fagos de la colección suiza. Harms no sabe si han salvado vidas humanas o plantas, ya que los estudios pertinentes no se han publicado todavía. Pese a todo, saber que los bacteriófagos recogidos en el Rin en Basilea —la mayor parte en el marco de un proyecto sin grandes recursos financieros— se utilizan para proyectos de investigación en lugares tan lejanos como Australia o Estados Unidos genera “una sensación especial”, reconoce.
“Quiero compartir nuestros fagos con todas las personas interesadas de cualquier parte del mundo. Así es como funciona la ciencia”, manifiesta Harm.
Adaptado del italiano por Lupe Calvo

En cumplimiento de los estándares JTI
Mostrar más: SWI swissinfo.ch, certificado por la JTI
























Puede encontrar todos nuestros debates aquí y participar en las discusiones.
Si quiere iniciar una conversación sobre un tema planteado en este artículo o quiere informar de errores factuales, envíenos un correo electrónico a spanish@swissinfo.ch.